4-a 塩化銅と亜酸化銅のエネルギー帯
投稿日 : 2021.12.18
塩化銅(CuCl)と亜酸化銅(Cu2O)の結晶は、立方晶とよばれる結晶系に属し、塩化銅は閃亜鉛鉱型、亜酸化銅は赤銅鉱型構造と呼ばれる構造をしていて、立方体の形の単位包(ユニットセル)が3次元的に繰り返されています。
それぞれの単位包には銅と塩素または酸素の原子が含まれていて、各原子の電子はパウリの排他律に従って次のような状態に収まっています。括弧の肩の数字がその軌道を占めている電子の数で、全部を足し合わせると原子番号になり、原子核に含まれる陽子の数と同じです。
8O : (1s)2 [(2s)2 (2p)4 ]
17Cl : (1s) 2 [(2s) 2 (2p) 6] [(3s) 2(3p) 5]
29Cu: (1s)2 [(2s)2 (2p)6 ] [(3s)2(3p)6(3d)10 ] (4s)1
それぞれの結晶で、原子間の距離や配置が違っているのでポテンシャルの重なりも違い、電子のエネルギー帯の様子も違ってきます。それでも、結晶構造が似ているために励起子に関係する波数の小さい領域での電子のエネルギー帯は似ていて、比較的簡単です。これがこの物質が励起子の分光学的研究が盛んにおこなわれてきた理由の一つです。
次の図は塩化銅と亜酸化銅のエネルギー帯の内、後の話に直接関係する部分をスケッチしたものです。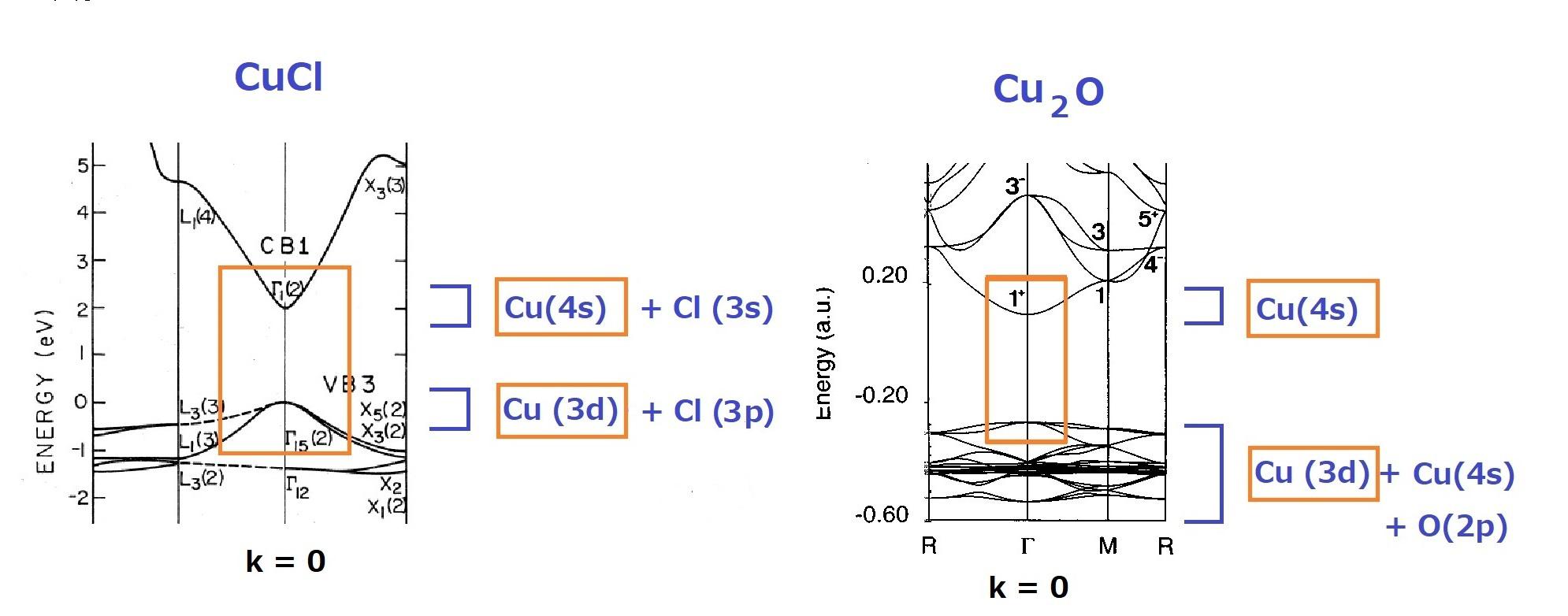 オレンジ色で囲んだ部分を見ると、下側のバンドは上に凸で、その波動関数は主に銅の3dで10個の電子で埋まっています。上側のバンドは下に凸で波動関数は主に銅の4s状態ですが、全部は埋まっていません。これら二つのバンドのエネルギー差が最も小さい波数はどちらもゼロで、そのエネルギー差がバンドギャップです。
オレンジ色で囲んだ部分を見ると、下側のバンドは上に凸で、その波動関数は主に銅の3dで10個の電子で埋まっています。上側のバンドは下に凸で波動関数は主に銅の4s状態ですが、全部は埋まっていません。これら二つのバンドのエネルギー差が最も小さい波数はどちらもゼロで、そのエネルギー差がバンドギャップです。
従って、バンドギャップエネルギーより小さなエネルギーのフォトンを下のバンドの電子が吸収しようとしても、行先がないので遷移できません。このバンドは価電子帯と呼ばれます。一方、バンドギャップ以上のエネルギーのフォトンでは、上のバンドには空席があるので遷移ができて、もし電界があれば加速されて電流が流れます。そのため、この電子は伝導電子とも呼ばれ、バンドも伝導帯と呼ばれます。
注:ΓとかXとかは、群論という数学の理論を応用した結晶の幾何学的構造から決まる波数空間の特別な位置を表す記号です。またΓ1とかΓ12とかはその位置での対応する電子の波動関数の幾何学的特徴を表わす規約表現といわれるものです。この既約表現は、ある量がゼロかゼロでないかを数値の計算をしなくても判定できたり、違った波動関数が重なった時に、どのような幾何学的な特徴をもった波動関数に分解して整理できたりできる便利な性質を持っていて、この数学の技は、固体物理だけでなく物理学全般で広く活用されています。ここでは専門的になるのでこれ以上の説明は省略します。
右の図のAは前の図のオレンジで囲んだ部分を簡略に示したものです。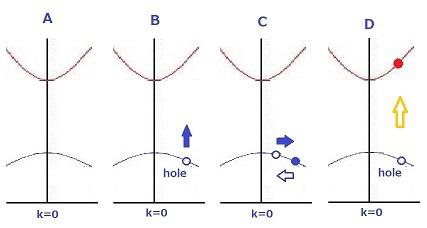 上が伝導帯の底、下が価電子帯の頂上辺りで、エネルギーはいずれもkに対しておおよそ放物線で表されます。そのため伝導電子は正の有効質量を持ち、価電子帯の電子は負の有効質量をもちます。
上が伝導帯の底、下が価電子帯の頂上辺りで、エネルギーはいずれもkに対しておおよそ放物線で表されます。そのため伝導電子は正の有効質量を持ち、価電子帯の電子は負の有効質量をもちます。
図のBは価電子帯の一個の電子が何かの事情でなくなり、まるで泡ができたようになったものです。この泡はプラスの電気を帯びて周りの電子を呼びよせ、Cはその泡の位置に別の電子が入った状態です。DはBがフォトンの吸収によって起きた場合で、電子は赤丸のエネルギーを持ちます。
この現象を理論的に扱うにはすべての電子の状態を考慮してエネルギーを正しく見積もらなくてはならないのですが、この泡が電子と逆の電荷を持ち常に電子と逆に行動し、マイナスのエネルギーを持っていると考えることで代えられ、この見かけの量子を、電子に対する反物質の陽電子のように見做なすことができるようになります。これは正孔(hole)と呼ばれ、半導体の電気現象や光学現象をうまく説明するのに便利になります。この考えの有効性はトランジスターなどが作られていることで実証されています。

コメント